Demande d'échantillon
Vous souhaitez vous en rendre compte par vous-même ? Demandez un échantillon gratuit.
FAQ
Généralités
À quoi servent les concentrateurs UF FastGene ?
Ils sont utilisés pour la concentration, le dessalage et l’échange de tampon de biomolécules telles que les protéines, les acides nucléiques et les virus. Ils peuvent également servir à clarifier des échantillons ou à éliminer de petits contaminants.
Quelles tailles et quels MWCO sont disponibles ?
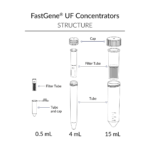
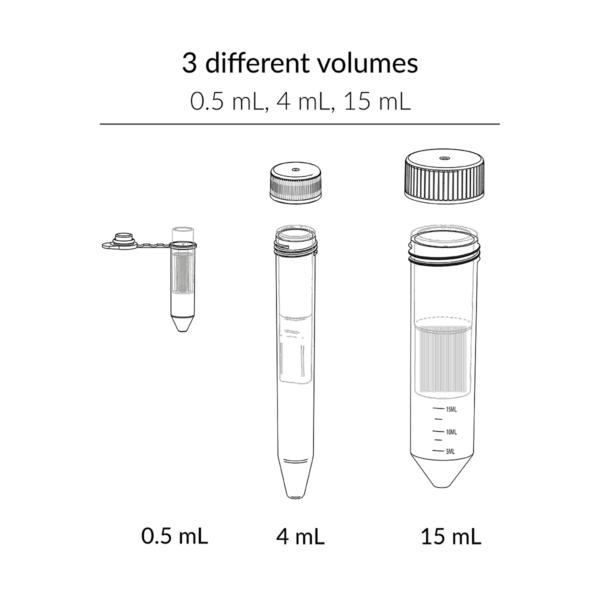
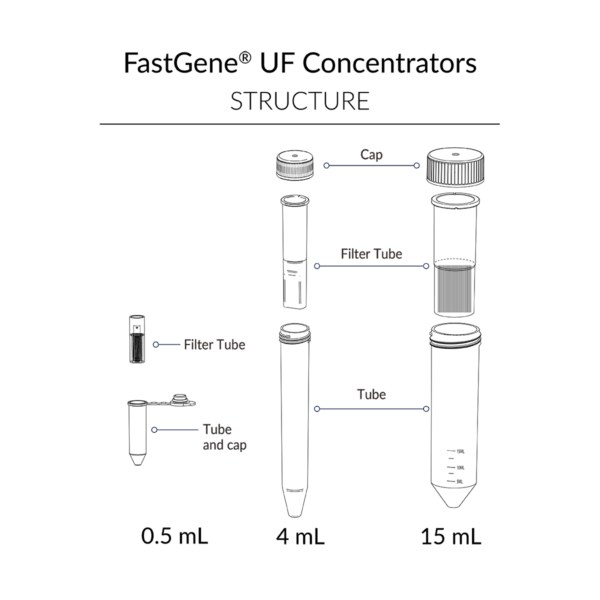
Les concentrateurs UF FastGene® sont proposés en trois tailles – 0,5 ml, 4 ml et 15 ml – chacune avec trois seuils de coupure moléculaire (MWCO) : 10 kDa, 30 kDa et 100 kDa.
Quel matériau de membrane est utilisé ?
Tous les concentrateurs UF FastGene® utilisent une membrane PES (polyéthersulfone) à faible liaison, idéale pour les protéines et les acides nucléiques.
Quelle plage de pH peuvent-ils supporter ?
La membrane PES est compatible avec un pH compris entre 1 et 14, couvrant ainsi la plupart des applications biologiques et chimiques.
Puis-je réutiliser les concentrateurs ?
Tous les concentrateurs UF FastGene® sont des dispositifs à usage unique et non stériles. La réutilisation peut réduire les performances et présenter un risque de contamination. La réutilisation n’est pas recommandée.
Peuvent-ils être stérilisés ?
Ne pas passer à l’autoclave. Pour le nettoyage ou une stérilisation limitée, vous pouvez rincer à l’éthanol à 70 % pendant 30 minutes avant utilisation. Laissez toujours l’éthanol s’évaporer complètement.
Les concentrateurs sont-ils exempts de RNase ou d’endotoxines ?
Ils ne sont pas certifiés exempts de RNase ou d’endotoxines. Si nécessaire, rincez-les avec une solution de DEPC à 0,1 % à 37 °C pendant 2 h, puis lavez-les soigneusement à l’eau ultra-pure.
Ces dispositifs sont-ils chimiquement compatibles avec les solvants organiques ou les réactifs puissants ?
Ils sont destinés à être utilisés avec des solutions aqueuses et biologiques.
Vérifiez le tableau de compatibilité chimique (voir le manuel d’utilisation ou la liste ci-dessous) avant d’utiliser des acides, des bases ou des solvants.
| Catégorie |
Produit chimique / Réactif |
Concentration maximale |
|
Catégorie |
Produit chimique / Réactif |
Concentration maximale |
| Acide |
Acide sulfamique |
≤3 % |
|
Solvant organique |
Benzène |
Non recommandé |
|
Acide formique |
≤5 % |
|
|
Acétone |
Non recommandé |
|
Acide acétique |
≤25 % |
|
|
Acétonitrile |
≤10 % |
|
Acide chlorhydrique |
≤1 M |
|
|
Toluène |
Non recommandé |
|
Acide sulfurique |
≤3 % |
|
|
Formaldéhyde |
≤5 % |
|
Acide nitrique |
≤10 % |
|
|
DMSO |
≤5 % |
|
Acide lactique |
≤5 % |
|
|
Acétate d’éthyle |
Non recommandé |
|
Acide phosphorique |
≤30 % |
|
|
Pyridine |
Non recommandé |
|
Acide trifluoroacétique |
≤10 % |
|
|
Chloroforme |
Non recommandé |
|
Acide trichloroacétique |
≤10 % |
|
|
Tétrachlorure de carbone |
Non recommandé |
| Base |
Hydroxyde de sodium
(tubes de 4 mL / 15 mL) |
≤0.5 M |
|
|
Tétrahydrofurane |
Non recommandé |
|
Hydroxyde de sodium
(tubes de 0.5 mL) |
≤0.1 M |
|
Autre réactif |
Phénol |
< 1 % |
|
Hydroxyde d’ammonium |
≤10 % |
|
|
Glycérol |
≤70 % |
| Alcool |
Méthanol |
≤60 % |
|
|
DTT |
≤0.1 M |
| |
Éthanol |
≤70 % |
|
|
DEPC (pyrocarbonate de diéthyle) |
≤0.2 % |
| |
Isopropanol |
≤70 % |
|
|
PEG (polyéthylène glycol) |
≤10 % |
| |
n-Butanol |
≤70 % |
|
|
Tampon phosphate (pH 8,2) |
≤1 M |
| |
|
|
|
|
Sulfate d’ammonium |
Saturé |
| |
|
|
|
|
Imidazole |
≤500 mM |
| |
|
|
|
|
Urée |
≤8 M |
| |
|
|
|
|
β-Mercaptoéthanol |
≤0.01 M |
| |
|
|
|
|
Tampon Tris (pH 8,2) |
≤1 M |
| |
|
|
|
|
Carbonate de sodium |
≤20 % |
| |
|
|
|
|
Chlorhydrate de guanidine |
≤6 M |
Utilisation
Puis-je les utiliser à 4 °C ?
Oui. La centrifugation à 4 °C est possible, mais la viscosité augmente à basse température ; il convient donc de prolonger la durée de centrifugation d’environ 1,5 fois la durée initiale.
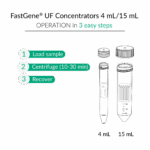
Comment récupérer l’échantillon concentré ?
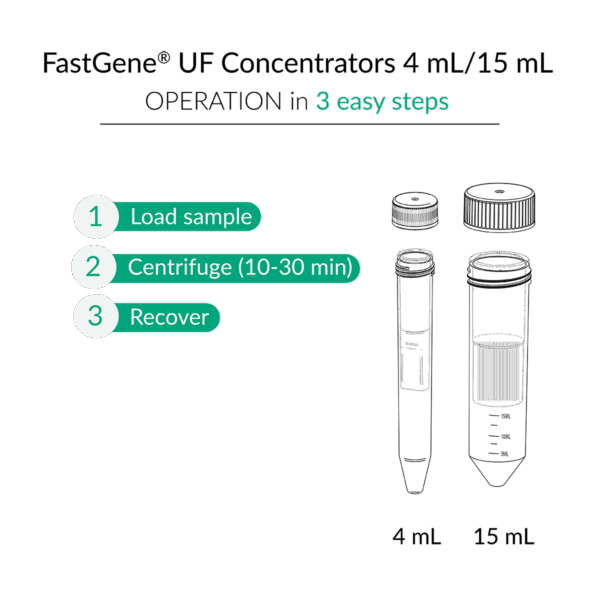
- Tubes de 0,5 mL : utilisez la méthode de centrifugation inversée – retournez le filtre dans un tube de collecte propre et centrifugez à 1 000 × g pendant 1 à 2 minutes.
- Tubes de 4 mL et 15 mL : récupérez le concentré directement à l’aide d’une pipette.
Comment puis-je améliorer la récupération des protéines ou éviter toute perte ?
- Choisissez un MWCO correspondant à environ un tiers du poids moléculaire de la protéine cible.
- Évitez une force centrifuge excessive ou des temps de centrifugation trop longs.
- Si l’échantillon est visqueux ou a tendance à coller, pré-bloquez la membrane avec 10 % de glycérol pendant une nuit et rincez-la avant utilisation.
Ces dispositifs peuvent-ils éliminer les détergents ou les endotoxines ?
- Détergents : Seulement partiellement ; l’efficacité diminue au-delà de la valeur CMC.
- Endotoxines : Non, car les endotoxines ont souvent une taille supérieure à 10 kDa et ne sont pas éliminées efficacement par ultrafiltration.
Les concentrateurs FastGene UF peuvent-ils être utilisés pour la concentration de virus ou de nanoparticules ?
Oui.
- Lentivirus : utilisez un MWCO de 100 kDa.
- Adénovirus : utilisez un MWCO de 50 kDa.
Ils conviennent également à la concentration de nanoparticules et d’exosomes (recommandé : 50–100 kDa).
Quels paramètres de centrifugation dois-je utiliser ?
- 0,5 mL : jusqu’à 14 000 × g
- 4 mL : jusqu’à 6 000 × g (3 000 × g pour 100 kDa)
- 15 mL : jusqu’à 5 000 × g (3 000 × g pour 100 kDa)
Utilisez des rotors à godets oscillants ou à angle fixe compatibles avec les tubes coniques standard. Équilibrez toujours vos échantillons.
Les échantillons s’assèchent-ils pendant la centrifugation ?
Non. Les concentrateurs UF FastGene® sont dotés d’une conception à volume mort qui empêche le séchage complet et protège votre échantillon.
Dépannage
Ma protéine s’est précipitée pendant la concentration — que dois-je faire ?
Une précipitation peut se produire si la concentration est trop rapide ou trop poussée. Essayez :
- De réduire la force centrifuge (à 30–50 % de la valeur recommandée).
- De passer à un MWCO plus élevé (par exemple, 30 kDa au lieu de 10 kDa).
- Mélanger délicatement l’échantillon entre les centrifugations.
Pourquoi ma protéine cible a-t-elle disparu après la centrifugation ?
Causes possibles :
- Le MWCO choisi est trop élevé (la cible a traversé le filtre).
- Force centrifuge trop élevée ou rotor non calibré.
- La protéine s’est précipitée pendant la centrifugation. Vérifiez le filtrat et le concentré ; si la protéine se trouve dans le filtrat, utilisez un MWCO plus faible
Seuls les clients connectés peuvent laisser un avis.







Note et avis
Il n’y a pas encore d’avis.